Die Zulassung von Sotorasib beim KRAS G12C-mutierten NSCLC basieren auf CodeBreaK-Studienprogramm, dessen einzelne Studien jährlich, so auch bereits in
diesem Jahr mit der Codebreak 101, die Kongresslandschaft beschäftigen. Beim diesjährigen ESMO wurde eine gepoolte Analyse aus diesem Studienprogramm vorgestellt.
Sotorasib beim KRAS G12C-mutierten NSCLC
Sotorasib long-term clinical outcomes in pretreated KRAS G12C-mutated advanced NSCLC: Pooled analysis from the CodeBreaK clinical trials – Skoulidis et al. #1305P
Für die vorgestellte Analyse wurden die Daten von insgesamt 467 Patient:innen aus den Studien CodeBreaK 100, CodeBreak 101, CodeBreak 105 und Codebreak 200 gepoolt und statistisch ausgewertet.
Das mediane Alter lag bei 65 und ca. 30 % hatten eine Vorgeschichte von Hirnmetastasen. Die Patient:innen hatten im Median bereits zwei Vortherapien erhalten, in denen fast alle bereits eine Immuntherapie (91,4 %) und eine platin-basierte Chemotherapie (93,6 %) bekommen haben.
Ergebnisse:
Wirksamkeit:
Bei einer medianen Nachbeobachtungszeit von 24,9 Monaten betrug das mPFS 5,6 Monate und war bei Patient:innen mit (4,9 Mo.) und ohne (5,9 Mo.) Vorgeschichte von Hirnmetastasen konsistent. Das mediane OS betrug 11,6 Monate. Sowohl Patient:innen mit (mOS: 10,2 Monate) als auch ohne (mOS: 12,9 Monate) Vorgeschichte von Hirnmetastasen profitierten von der Therapie. Die ORR nach BICR betrug 33,7 % und die mediane DOR lag bei 10,8Monaten.
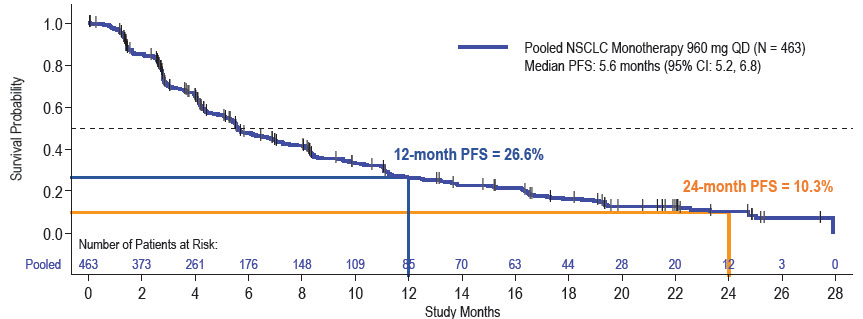
Abbildung 1 mPFS für die gepoolten CodeBreak-Studien
Verträglichkeit:
Das Verträglichkeitsprofil war über alle vier betrachteten Studien konsistent, mit einer niedrigen Rate an Dosisreduktionen oder Beendigungen der Behandlung aufgrund von TRAEs. Die häufigsten TRAEs (alle Grade) waren Diarrhoe (31,1%), erhöhtes ALT (12,4 %) und erhöhtes AST (12,2%). Grad ≥ 3 TRAEs wurden bei 147 (23,1 %) Patienten berichtet.
Die Präsentation können Sie
hier herunterladen.


