Beim EHA 2024 wurden aktualisierte Daten des Safety Run-Ins der Golden Gate Studie, Ergebnisse nach 43 Monate Follow-Up in der Hovon-146 Studie sowie erste Resultate zum Einsatz von Blinatumomab als Erstlinien-Therapie bei Patient:innen mit B-Zell ALL und „intermediate or high risk down syndrome“ vorgestellt.
Blinatumomab bei adulter B-ALL
BLINATUMOMAB ALTERNATING WITH LOW-INTENSITY CHEMOTHERAPY (LIC) IN OLDER ADULTS WITH NEWLY DIAGNOSED B-CELL ACUTE LYMPHOBLASTIC LEUKEMIA (ALL): SAFETY RUN-IN FOLLOW-UP FOR THE PHASE 3 GOLDEN GATE STUDY – Jabbour et al. P416
Die Phase-3 Golden Gate Studie (NCT04994717) untersucht die Kombination von Blinatumomab alternierend mit niedrig-intensiver Chemotherapie in älteren Patient:innen mit neudiagnostizierter B-Zell ALL.
Ergebnisse:
Wirksamkeit
Zum Zeitpunkt des Data-Cut-Offs (mediane Dauer auf Therapie: 6,7 Mo. [0,2-20,1]) beendeten 13 von 14 Patient:innen (medianes Alter 70 Jahre) Induktion 2 und fünf Patient:innen Konsolidierungszyklus 4. Zwei Patient:innen schlossen Erhaltungszyklus 11 ab.
Nach 14 Wochen erreichten 92,9% der Patient:innen eine CR, wobei 84,6% dieser Patient:innen ebenfalls eine MRD-Negativität erreichten (siehe Abbildung 1).
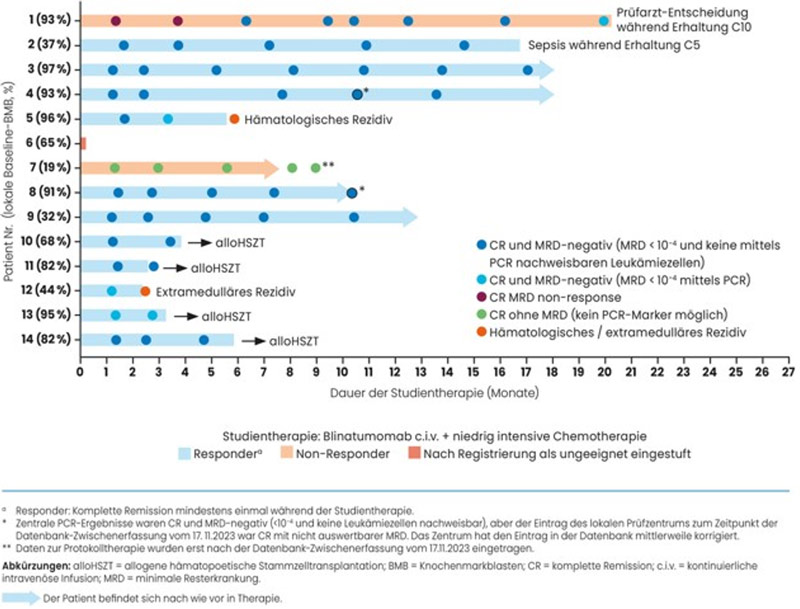
Abbildung 1 Therapieansprechen (Swimmer Plot) der Safety-Run-In Kohorte – nach Jabbour et al.
Verträglichkeit
Behandlungsbedingte unerwünschte Ereignisse ≥Grad 3 traten bei 85,7% der Patient:innen auf. Sechs Patient:innen hatten Blinatumomab-assoziierte neurologische unerwünschte Ereignisse vom Grad 1 oder 2, wobei alle bis auf ein Ereignis reversibel waren. Kein/e Patient:in hat Blinatumomab aufgrund einer neurologischen Nebenwirkung dauerhaft abgesetzt. Es wurden kein CRS ≥Grad 3 berichtet.
Fazit
Blinatumomab alternierend mit dosis-reduzierter Chemo zeigte ein akzeptables Verträglichkeitsprofil und war effektiv in älteren Patient:innen.
Hier können Sie das Abstract-Slide-Deck herunterladen.
BLINATUMOMAB ADDED TO PREPHASE AND CONSOLIDATION THERAPY IN ADULT B-ALL: A COMPARISON OF THE CONSECUTIVE HOVON-100 AND H-146 STUDIES – Rijneveld et al. S113
Die Hovon 146-Studie basiert auf einem pädiatrisch inspirierten Protokoll, das bereits in der Hovon 100-Studie zum Einsatz kam. Allerdings wurden die Dosen von Anthrazyklinen, MTX, Etoposid und PEG-ASP für Patient:innen ≥40 Jahre reduziert und Blinatumomab zur Präphase (14 Tage) sowie Intensivierung und Konsolidierung hinzugefügt.
Ergebnisse:
Wirksamkeit
Von 71 eingeschlossenen Patient:innen erreichten 58% bereits in der Präphase ein erstes Ansprechen. Nach dem ersten Zyklus der Konsolidierung erreichten 56/59 Patient:innen, die die Behandlung fortgeführt haben, eine CR. Das geschätze PFS und OS nach 4-Jahren lagen bei 57% (Ph+: 68%, Ph-: 49%) bzw. 76% (Ph+: 85%, Ph-: 70%).
Verträglichkeit
Die Häufigkeit von CRS Grad 3 in der Präphase betrug 21% (15/71) und die von Grad 3 ICANS 3% (2/71). Fünfzehn Patient:innen brachen die Therapie vor dem ersten Zyklus Blinatumomab-Konsolidierung ab.
Blinatumomab bei Patient:innen mit Down-Syndrom
BLINATUMOMAB FOR FIRST LINE TREATMENT IN INTERMEDIATE AND HIGH RISK DOWN SYNDROME B-CELL ACUTE LYMPHOBLASTIC LEUKAEMIA: INITIAL FINDINGS FROM THE ALLTOGETHER1 DS TRIAL – Samarasinghe et al. S111
Die ALLTogether1 DS-Studie testete zwei Zyklen Blinatumomab als Ersatz für eine Chemo-Konsolidierung bei Patient:innen mit Down-Syndrom (0-25J) und neu-diagnostizierter B-ALL, die nach der Induktion noch MRD-positiv waren.
Ergebnisse:
Wirksamkeit
Nach einem Zyklus Blinatumomab waren 91% (31/33) der Patient:innen MRD-negativ, am Ende von Zyklus 2 alle Patient:innen mit verfügbaren Daten. Nach einer medianen Nachbeobachtungszeit von 15 Monaten sind bislang keine Ereignisse (Tod/Rezidiv/sekundärer Krebs) aufgetreten.
Verträglichkeit
Trotz Prophylaxe mit Levetiracetam bei der Mehrzahl der Patient:innen (29/33) traten bei sechs Patient:innen Krampfanfälle auf. Dabei waren 5/6 Patient:innen älter als 10 Jahre. Fünf Patient:innen brachen die Therapie ab, zwei vor der MRD-Beurteilung am Ende von Zyklus 1 und drei danach.


